Na história da tabela periódica, um dos esforços mais antigos, no sentido de se encontrar uma relação no comportamento dos elementos, resultou na identificação e na reunião de elementos com propriedades semelhantes em grupos de três, denominados tríades.
Nessas tríades, a massa atômica de um elemento era aproximadamente a média aritmética dos pesos atômicos dos outros dois. Isto foi proposto pelo químico alemão J.W. Döbereiner, em 1829.
Vejamos algumas tríades.
Lítio – Sódio – Potássio
Cloro – Bromo – lodo
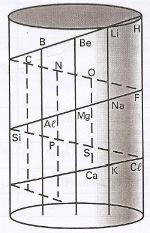
Em 1862, A. E. de Chancourtois ordenou os valores de massas atômicas ao longo de linhas espirais traçadas nas paredes de um cilindro, originando o parafuso telúrico, em que os elementos com propriedades semelhantes estavam reunidos numa mesma linha vertical.
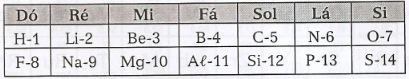
Em 1866, J. A. R. Newlands fez um arranjo dos elementos denominado lei das oitavas, porque, a partir de um dado elemento, o oitavo é uma espécie de repetição do primeiro, ou seja, o primeiro e o oitavo elementos teriam propriedades semelhantes.
Em 1869, Lothar Meyer e Dimitri Ivanovich Mendeleev, independentemente, criaram tabelas periódicas dos elementos (semelhantes à atual) onde os elementos eram dispostos em ordem crescente de massas atômicas. Essas tabelas foram criadas quando se conheciam apenas 63 elementos químicos.
Mendeleev organizou os elementos em linhas horizontais, chamadas períodos, e em linhas verticais, denominadas grupos, contendo estes elementos com propriedades semelhantes.
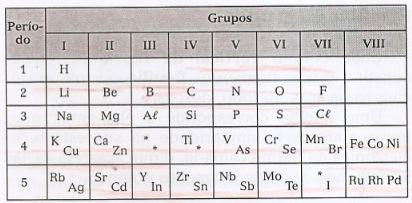
Nessa tabela, pode-se observar a existência de lacunas referentes a elementos não conhecidos, e de asteriscos (*), elementos que foram previstos por Mendeleev.
A classificação periódica elaborada por Mendeleev foi utilizada até 1913, quando Moseley verificou que as propriedades dos elementos eram dadas pela sua carga nuclear (número atômico – Z). Com esta descoberta foi possível corrigir algumas anomalias observadas por Mendeleev.
| Tabela periódica atual: Os elementos são agrupados em ordem crescente de número atômico (Z), observando-se a repetição periódica de muitas de suas propriedades. |