O ar possui, aos olhos da física, uma série de características e propriedades. Elas afetam diretamente a forma com que interagimos com o ar, e explicam uma série de fenômenos que afetam a nossa vida diária. As principais propriedades do ar, quando estudamos esse fluido na física, podem ser resumidas nos itens a seguir.
Incolor, inodoro e insípido
No sentido humano, a primeira coisa que podemos constatar a respeito do ar é aquilo que podemos medir com os nossos órgãos do sentido, tanto a visão, quanto o paladar e o olfato. Lembremos, no entanto, que o ar, como qualquer fluido, pode possuir partículas e elementos em dispersão – como gases, fumaça e poeira. Contudo, por definição e observação, podemos dizer que o ar:
- É incolor, pois não pode ser visto
- É inodoro, pois retiradas partículas em dispersão não sentimos seu odor
- É insípido, pois não sentimos sabor em nossa boca quando respiramos
Massa e volume
Se utilizarmos outro de nossos órgãos do sentido, o tato, não conseguimos de forma alguma sentir o “peso” do ar, ou mesmo “pegá-lo”. Ainda assim, como acontece com a água, o ar possui massa e volume. Algumas experiências simples podem demonstrar isso: o ar ocupa espaço e possui certo volume.
Se sopramos ar dentro de uma bexiga, ela enche. Em outras palavras – o ar que expelimos para dentro da bexiga ocupa espaço, logo tem volume. Em relação à massa, se notarmos bem, bexigas que enchemos com o ar dos pulmões nunca sobem desenfreadamente. Isso ocorre porque na expiração, adicionamos ao ar que expelimos água, gás carbônico e outras partículas, que possuem massa maior que o ar que inspiramos (esse basicamente constituído de nitrogênio e oxigênio). Como o ar que soltamos é mais “pesado” que o ar normal, a bexiga desce.
Outro modo de constatar o “peso do ar” é utilizar uma balança feita com uma régua, como demonstrado no esquema a seguir. A bexiga cheia é mais pesada que a vazia, o que demonstra que a massa do ar existe no interior da bexiga cheia.
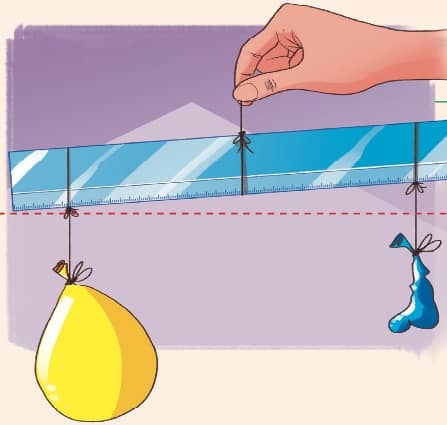
Pressão atmosférica
Por ter massa e volume, o ar que constitui a atmosfera sofre o efeito da gravidade. Ou seja, a enorme massa de ar que constitui a atmosfera, a despeito de ser um amontoado de gases, tende a “cair” em direção ao solo. O peso dessa massa de ar sobre nós exerce determinada pressão.
Como a superfície da Terra não é plana e regular, dependendo do lugar onde estamos a atmosfera pode ter maior ou menor espessura. Por exemplo: se estivermos na praia, ou seja, ao nível do mar, a pressão da atmosfera tende a ser maior. Em grandes altitudes, como ocorre em cidades como Cusco, no Peru, ou Quito, no Equador, ambas a mais de 3000m de altitude, a pressão do ar é muito menor.
Há um modo mais simples de compreender. No caso do ar, como não “sentimos” o seu peso, é difícil visualizar essas diferenças. O mesmo não ocorre no caso da água. Como bem sabemos, quanto maior a profundidade atingida por um mergulhador, mais a pressão. Alguém que mergulhe a 30m ou 40m de profundidade precisa fazer descompressões ao retornar à superfície. Para profundidades maiores, mergulhadores usam escafandros (trajes equipados com proteções e resistentes à pressão).
Quando chegamos à casa de centenas de metros de profundidade, é apenas possível mergulhar dentro de pequenos submarinos (em geral chamados de “batiscafos“). Ou seja, quando maior a profundidade, maior o “peso” da água sobre o seu corpo – ou a pressão. Quando estamos a 100m de profundidade no mar, é como se nosso corpo sustentasse uma coluna de água de 100m de altura em peso – ou seja, toneladas de água sobre nosso corpo.
É possível medir a pressão atmosférica com um instrumento proposto inicialmente pelo físico e matemático italiano Evangelista Torricelli (1608-1647), chamado barômetro.
Compressibilidade e expansibilidade
Assim como ocorre com toda a matéria, o ar possui propriedades gerais – entre elas a compressibilidade e a expansibilidade. O ar pode ser comprimido – quando exercemos pressão ou força externa, fazemos com que as moléculas no ar se aproximem umas das outras, e elas tendem a ocupar menos espaço.
Quando isso ocorre, a proximidade entre as moléculas eleva chances de colisão e aumenta a pressão reversa do ar. Em outras palavras, toda a força que colocamos para comprimir o ar é devolvida em reação pelo ar comprimido, que passa a exercer uma pressão em direção ao exterior.
Complicado? Então pense numa bola de futebol ou no pneu de uma bicicleta. O ar que injetamos na bola ou no pneu é, se usarmos uma bomba de posto de gasolina, comprimido. Se você bem se lembra, temos inclusive de ajustar a pressão do ar conforme o que vamos encher.
Quando enchemos o pneu ou a bola, eles tomam forma e ficam duros. Essa “dureza” é exatamente a força que o ar, comprimido dentro desses objetos, mantém ininterruptamente contra as paredes da bola ou do pneu. Se apertamos o pininho no bico de um dos dois, o ar escapa de forma violenta, pois a pressão interna naquele ponto foi aliviada.
Essa força para “escapar” demonstra a propriedade de expansibilidade do ar, ou elasticidade desse material. Enquanto as forças que mantém o ar comprimido permanecem, ele cria pressão em sentido inverso. Quando as forças externas são retiradas, o ar tende a voltar ao seu volume original, em rápida expansão.
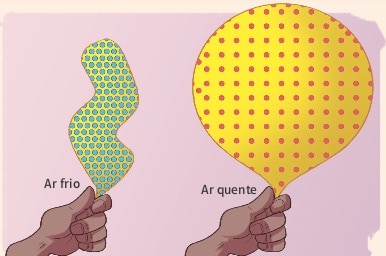
Finalmente, a temperatura é, em termos físicos, a agitação das moléculas de um material. E, quando a matéria está mais quente, ela acaba tendendo a ocupar mais espaço. De volta à bexiga – quando você enche uma bexiga com ar quente, ela tende a subir ou manter-se no ar por mais tempo. Uma bexiga enchida com ar frio dificilmente consegue, manter a sua forma, e tende a cair.
Esse último experimento simples, como mostra a imagem, explica fenômenos atmosféricos de grande complexidade, como as massas de ar e “frentes frias”, chuvas e tempestades e até mesmo furacões, ciclones e tornados.
Por: Carlos Artur Matos